INTRODUÇÃO
As doenças obstrutivas crônicas das vias aéreas (p. ex. fibrose cística, bronquite crônica) são caracterizadas fisiopatologicamente por episódios infecciosos e inflamat órios que resultam em acúmulo de secreções mucosas espessas e viscoelásticas, o que acarreta redução na efic ácia dos mecanismos mucociliar e de tosse para eliminar o fluido estagnado1. Os constituintes essenciais da secreção brônquica podem ser divididos em três grupos, como se mostra na Tabela 1. No tratamento da doença brônquica obstrutiva e inclusive da sinusite, com a finalidade de auxiliar e eventualmente dispersar o uso de antibióticos, uma das vertentes é a melhora da depuração mucociliar através da redução da viscosidade e da elasticidade do muco.
Os principais enfoques neste sentido mostram uso de irrigações com soluções salinas, de estimulantes mucociliares (p. ex.,trifosfato de adenosina), e dos chamados muco-reguladores ou mucolíticos.
Conforme a data da entrada na clínica, estes fármacos podem ser classificados em 4 grupos:
1. Década de 60: N-Acetilcisteína
2. Década de 70: Carboximetil-cisteína
3. Década de 80: Ambroxol
4. Década de 90: Erdosteína
N-ACETILCISTEÍNA
Primeiro agente proposto como "mucolítico", a Nacetilciste ína mostrou utilidade clínica durante muitos anos de uso em uma série de distúrbios respiratórios. Recentemente, foi verificado que pode apresentar efeitos ben éficos em condições caracterizadas por diminuição das reservas de glutationa reduzida (GSSH) ou de estresse oxidativo (p.
ex., em infecção pelo vírus HIV, câncer, cardiopatia e tabagismo)2.
Não obstante, o preciso mecanismo da ação mucolítica era indefinido, e o efeito clí- nico não podia ser reproduzido com facilidade em laborat ório.
De fato, a administração de N-acetilcisteína ou de S-carboximetilcisteína a cobaias não provocou alteração das propriedades reológicas ou bioquímicas da secreção mucosa brônquica3. Dúvidas quanto à real utilidade clínica da N-acetilcisteína aparecem em publicações esparsas na literatura especializada, mostrando, por exemplo, inefic ácia do fármaco quanto aos níveis de glutationa, aos produtos de peroxidação lipídica, ao muco tráqueobr ônquico ou mesmo à condição clínica4.
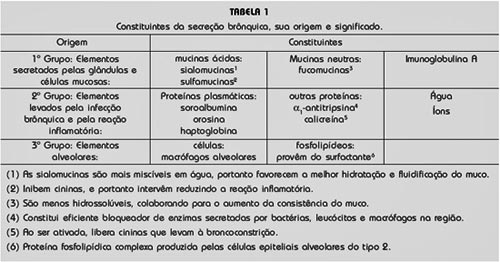
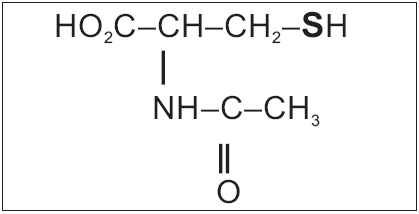
Figura 1. Molécula da N-acetilcisteína, mostrando o grupo tiol em negrito, que está "livre"
(compare com a Figura 2).
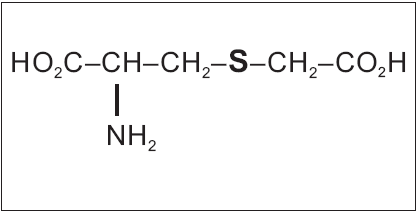
Figura 2. Molécula de carboximetil-cisteína, mostrando o grupo tiol em negrito, que está "protegido".
CARBOXIMETIL-CISTEÍNA
Diversos estudos envolvendo bronquite obstrutiva em desenho duplo-cego com placebo deixaram suficientemente claro que a carboximetil-cisteína, administrada em forma de xarope, durante 3 semanas (2,25 g/dia), causa modificações significativas nas propriedades físico-quí- micas do muco, provocando aumento da depuração mucociliar e melhora na eficácia da tosse5.
Curiosamente, porém, os volumes expectorados elevavam-se apenas nas 3 primeiras semanas de uso do fármaco. Os efeitos da carboximetil-cisteína têm sido atribuí- dos à lise do muco por ação dos grupamentos tiólicos livres do fármaco, quando aplicado diretamente sobre esse muco6. Nesta concepção, os efeitos modificadores do muco causados pela carboximetil-cisteína só poderiam manifestar- se após metabolização e conseqüente liberação dos grupamentos sulfidrila, os quais se apresentam bloqueados na molécula original (v. Figura 2). Tais grupamentos, então liberados nos metabólitos do fármaco, reduzem as pontes de dissulfeto constituintes das proteínas secretoras7. Apesar da plausibilidade desta explicação, porém, em seres humanos não foi possível demonstrar biotransformação apreciável do fármaco, pois mais de 80% da dose administrada por via oral pode ser recuperada na urina sem modificação8.
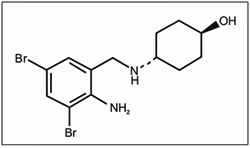
Figura 3 . Molécula do ambroxol.
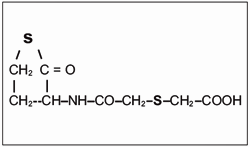
Figura 4 . Molécula da erdosteína, mostrando os grupos tiólicos em negrito.
AMBROXOL
O ambroxol é agente "mucorregulatório" de ação mista sobre a síntese e a composição do muco e sobre a mucosa das vias aéreas superiores9, usado amplamente no tratamento da bronquite crônica, com resultados clínicos inconsistentes10.
A observação de que o ambroxol apresenta efeito inibitório pH-dependente sobre o crescimento de Mycobacterium tuberculosis adicionaram cré- dito aos relatos dos efeitos benéficos do fármaco na terap êutica da tuberculose11.
Além disto, tanto in vitro como in vivo, o fármaco mostrou efeito antiinflamatório, atrav és da redução da liberação de citocinas como o TNF-a (fator de necrose tumoral a), a IL-2 (interleucina-2) e o IFg (interferon-g)12.
Por outro lado, não só a atividade protetora do ambroxol contra produtos de peroxidação lipídica (dienos conjugados, hidroperóxidos lipídicos, dialdeído malônico, bases de Schiff) não pôde ser demonstrada convincentemente, como também o fármaco isoladamente parece poder atuar como pró-oxidante13. Ademais, não parece haver efeito importante sobre a atividade mucociliar14.
ERDOSTEÍNA
A erdosteína é derivado tiólico do aminoácido metionina, contendo 2 átomos de enxofre bloqueados, um dos quais na cadeia lateral alifática, e o segundo por inclusão no anel heterocíclio tiolactônico (Figura 4). Aspecto distinto deste fármaco é que, após metabolização hepática, são liberados pelo menos 3 metabólicos, todos ativos farmacologicamente. As principais propriedades farmacológicas da erdosteína podem ser assim resumidas:
ESTUDOS CLÍNICOS GERAIS
Resultados de estudos clínicos indicaram que a administra ção oral de erdosteína, em doses de 600 a 900 mg/ dia, causa sensível melhora em pacientes com distúrbios pulmonares envolvendo espessamento do muco tráqueobr ônquico e alteração de suas características físico-quí- micas15. Na dose de 300 mg duas vezes ao dia a pacientes com bronquite hipersecretória crônica estável, em compara ção com placebo, a erdosteína diminuiu significativamente a freqüência e a intensidade da tosse, e aliviou os sintomas de dificuldade respiratória e dispnéia16. Um outro estudo mostrou que a eficácia clínica de 300 mg de erdosteína 2 vezes ao dia foi ao menos equivalente àquela de 30 mg de ambroxol duas vezes ao dia em um estudo duplo-cego em 29 pacientes portadores de broncopneumopatia aguada ou crônica exacerbada tratados durante 7 dias. A erdosteína reduziu mais efetivamente do que o ambroxol a adesividade do escarro (redu ção de 89 versus 60% em comparação entre o período basal e o final do tratamento)15.
PROPRIEDADES ANTIOXIDANTES
As propriedades antioxidantes da erdosteína são ilustradas por sua capacidade de reduzir as concentrações séricas de dialdeído malônico, que estão cronicamente elevadas em fumantes17 e constituem bom indicativo de peroxidação lipídica, ou seja, conseqüência de lesões oxidativas causadas por agressão farmacológica. Este efeito é devido aos metabólitos ativos, pois apenas após administração in vivo a erdosteína demonstrou redução do desenvolvimento do edema de pata em ratos provocado pela injeção de FeCl2,um indutor de radicais livres18. In vitro, demonstrou-se que a erdosteína tem ação contra a inativação da a1-antitripsina causada por exposi ção direta à fumaça do cigarro19. Estaação pôde também ser demonstrada in vivo, em ratos expostos à fuma- ça do cigarro20. Além disto, em camundongos, a erdosteína pode diminuir a toxicidade do paraquat (droga que induz formação de radicais reativos do oxigênio e leva à insufici ência respiratória progressiva e irreversível)21.
ATIVIDADES MUCOLÍTICA E MUCOCILIAR
Em portadores de broncopneumonia aguda ou crônica exacerbada, o tratamento durante 7 dias com erdosteína (300 mg, duas vezes ao dia) produziu maior redução na adesividade do escarro que o ambroxol22. A atividade mucociliar positiva da erdosteína foi demonstrada em 16 pacientes previamente fumantes, portadores de bronquite crônica, tratados durante 8 dias com 300 mg do fármaco, duas vezes ao dia. A taxa de transporte mucociliar mensurada após foi 56% superior ao período anterior ao tratamento (antes = 4,6 mm/min; depois = 7,2 mm/min)23. CONCLUSÃO A erdosteína é derivado tiólico com propriedades muco-moduladoras e antioxidantes.
Os estudos em modelos animais e em humanos demonstraram sua capacidade de modulação da produção e da viscosidade do muco, e de aumentar transporte mucociliar.
Foi também demonstrado que a erdosteína antagoniza os efeitos negativos da liberação de radicais livres do tabagismo sobre a atividade a1-antitripsina.
Através da redução da viscosidade das secreções brônquicas e/ou redução da inflamação brônquica, a erdosteína facilita a penetração de antibióticos no escarro24, acarretando concentração antibiótica local mais elevada e resposta clínica mais rá- pida. Os resultados de estudo clínico demonstraram que a erdosteína, administrada por via oral, constitui tratamento eficaz e adequadamente tolerado por pacientes portadores de doença brônquica obstrutiva crônica.
Foi demonstrado que a eficácia do fármaco é significativamente superior à do placebo e no mínimo igual à do ambroxol na melhora dos sintomas.
É importante salientar que um estudo clínico adequadamente controlado forneceu evidências convincentes de que a erdosteína melhora a eficácia da amoxicilina no tratamento da exacerba ção infecciosa aguda da bronquite obstrutiva crô- nica25, sem qualquer aumento na incidência de efeitos colaterais adversos15. O perfil favorável de tolerabilidade da erdosteína pode ser justificado pela presença de seus grupamentos sulfidrila quimicamente bloqueados (v.Figura 4).
Os radicais sulfidrila são liberados após metabolização hepá- tica da molécula, exercendo subseqüentemente sua atividade mucolítica e varredora de radicais livres em nível brônquico. Desta forma, a erdosteína não apresenta quaisquer efeitos deletérios sobre a mucosa gástrica26.
REFERÊNCIAS BIBLIOGRÁFICAS
1. Brow DT . Carbocysteine. Drug Intell. Clin. Pharm. 22: 603-608, 1988.
2. Kelly GS . Clinical applications of N-acetylcysteine. Altern. Med. Rev. 3: 114-127, 1998.
3. Livingstone CR et al. . Model systems for the evaluation of mucolytic drugs: acetylcysteine and Scarboxymethylcysteine. J. Pharm. Pharmacol. 42: 73-78, 1990.
4. Konrad F et al. . The application of nacetylcysteine as an antioxidant and mucolytic in mechanical ventilation in intensive care patients. A prospective, randomized, placebo-controlled, doubleblind study. Anaesthesist 44: 651-658, 1995.
5. Ailward M et al. . Clinical evaluation of carbocisteine in the treatment of patients with chronic bronchitis. A double-blind trial with placebo control. Clin. Trials. J. 22: 36-44, 1985.
6. Sheffener AC . The reduction in vitro in viscosity of mucoprotein solution by a new mucolytic agent, N-acetyl-cysteine. Ann. N. Y. Acad. Sci. 106: 298-312, 1963.
7. Quevauvillier A et al. . Activité des mucolytiques sur la rétention experimentale du mucus intrabronchiques chez de rat. Therapie 22: 485-493, 1967.
8. Waring RH & Mitchell SC . The metabolism and elimination of S-carboxymethyl-cysteine in man. Drug Metab. Disp. 10: 61-62, 1982.
9. DePrá M & Oberti F . Childhood sinusitis. A description and comments based on a 10-year series of cases. Minerva Pediatr. 37: 515-530, 1990.
10. Guyatt GH et al. . A controlled trial of ambroxol in chronic bronchitis. Chest 92: 618-620, 1987.
11. Grange JM & Snell NJ . Activity of bromhexine and ambroxol, semi-synthetic derivatives of vasicine from the Indian shrud Adhatoda vasica, against Mycobacterium tuberculosis in vitro. J. Ethnopharmacol. 37: 49-53, 1996.
12. Pfeifer S et al. . Reduction of cytokine release of blood and brochoalveolar mononuclear cells by ambroxol. Eur. J. Med. Res. 2: 129-132, 1997.
13. Piotrowski WJ et al. . Effect of paraquat intoxication and ambroxol treatment on hydrogen peroxide production and lipid peroxidation in selected organs of rat. J. Appl. Toxicol. 16: 501-507, 1996.
14. Scuri R et al. . Mucolytic agents and mucociliary activity. Rhinology 16: 223-231, 1984.
15. Dechant KL & Noble S . Erdosteine Drugs 52: 875-881, 1996.
16. Ghiringhelli G & Mancini C . Cross-over clinical study efficacy and tolerability of erdosteine in the treatment of chronic obstrutive bronchial disease in stable hypersecretive phase controlled double blind study vs placebo. Arch. Med. Interna 47: 113-120, 1995.
17. Mancini C et al. . Erdosteine effect on serum malondialdehyde of healthy smokers and nonsmokers. A pilot study. Eur. Resp. J. 10 (Suppl. 25): 95s, 1997.
18. Mancini C et al. . Erdosteine and its metabolites as antioxidants in the FeCl2-induced rats paw oedema. Eur. Resp. J. 10 (Suppl. 25): 314s, 1997.
19. Gazzani G et al. . In vitro protection by erdosteine against oxidative inactivation of alpha-1-antitrypsin by cigarrette smoke. Respiration 55: 113-118, 1989.
20. Biagi GL et al. . Erdostein protection from cigarrette smoke-induced loss of alpha-1-antitrypsin activity in rat lungs. Int. J. Clin. Pharmacol. Therap. Toxicol. 27: 235-237, 1989.
21. Kaise T et al. . Effects of KW-9144 on paraquat toxicity in mice and bleomycin-induced pulmonary injury in rats. Japn. J. Pharmacol. 61 (Suppl. 1): 81P, 1993.
22. Fumagalli G et al. . Erdostein: a new molecule with mucolytic activity. Clinical and instrumental evaluation in patients with acute and exacerbated chronic bronchopneumopathies. G. Ital. Mal. Torace 42: 299-308, 1988.
23. Olivieri D et al. . Activity of erdosteine on mucociliary transport in patients affected by chronic bronchitis. Respiration 58: 91-94, 1991.
24. Ricevuti G et al. . Influence of erdosteine, a mucolytic agent, on amoxycilin penetration into sputum in patients with an infective exarcebation of chronic bronchitis. Thorax 43: 585-590,1988.
25. Marchioni CF et al. . Evaluation of efficacy and safety of erdosteine in patients affected by chronic bronchitis during an infective exacerbation phase and receiving amocillin as basic treatment. Int. J. Clin. Pharmacol. Ther. Toxicol. 33: 612-618, 1995.
26. DeGiovanni L et al. . Lack of gastric adverse effects of erdosteine in rats and man. Int. J. Clin. Pharmacol. Ther. Toxicol. 29: 269-273, 1991.
27. Korolkovas A . Dicionário Terapêutico Guanabara . Farmacos do aparelho respiratório 11.6,1998/1999.
28. Zanini . Oga . Guia de Medicamentos 97/98 . Atheneu Ed. S. Paulo . Convêncio USP DI®.
1- Professor Doutor do Departamento de Farmacologia do ICB-USP; Médico do Serviço de Radiosótopos do Hospital da Beneficência Portuguesa de São Paulo.
2- Professor Doutor do Departamento de Farmacologia do ICB-USP.